近日,我院杭纬教授课题组在单细胞质谱成像研究方面取得进展,相关成果以“Single-Cell Mass Spectrometry Imaging of Multiple Drugs and Nanomaterials at Organelle Level”为题发表于ACS Nano(DOI: 10.1021/acsnano.1c02922)。
探究化学物质在生物组织甚至单细胞内的位置分布是生命科学研究的重要方向之一。特别是随着金属元素组学和元素标记技术的发展,对于元素的分析检测显得愈加重要。电感耦合等离子体质谱(ICP-MS)技术是最常用的元素检测手段之一,通过与激光剥蚀(LA)采样方法的联用,使得这种传统的溶液进样质谱技术具有了原位分析和化学成像的能力。但是,由于衍射极限以及透镜数值孔径等因素的限制,这种激光采样方法的空间分辨能力仍然停留在微米级别,难以应用于单/亚细胞水平上的成像研究。
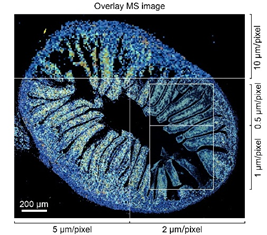
杭纬课题组首次设计了具有三通结构的样品剥蚀池,从而将微透镜光纤激光采样技术与ICP-MS相结合,搭建了LA-ICP-MS成像平台,该装置可以实现低至400纳米空间分辨率的质谱成像,对生物组织和单细胞内的多种化学物质进行可视化探测,还易于实现可调分辨率的成像模式。以同一片小鼠小肠剖面组织为研究对象,获得了从500纳米至10微米空间分辨率的药物分布成像图片。利用高分辨模式的成像,能够更直观、精准地描绘出小肠组织内微小的细节和药物的分布,从而揭示小肠对药物的吸收和作用机理。
这种高空间分辨率的LA-ICP-MS成像装置也可以在细胞器水平上实现对单细胞的成像分析。课题组将HeLa细胞与金纳米棒、卡铂等药物同时培养,而后将在石英片上贴壁生长的细胞放入样品剥蚀池内进行成像检测。结果表明金纳米棒主要位于细胞的溶酶体内,而金纳米棒上修饰的不同基团会影响细胞对纳米材料的摄取量、细胞的形貌以及活性产生;而卡铂药物被癌细胞摄取后主要分布在细胞核内,通过与核内DNA的相互作用诱导癌细胞凋亡。这种纳米级空间分辨的元素成像有望在生物学与医学等多领域获得应用,在纳米尺度下揭示待测物的化学物质分布。
该工作是在杭纬教授指导下完成的。实验部分主要由我院2017级博士研究生孟一凡(已毕业)完成,高超鸿、陆桥等参与了论文的研究工作。研究工作得到国家自然科学基金(项目批准号:21974116、21521004、22027808)的资助和支持。
论文链接: https://doi.org/10.1021/acsnano.1c02922
